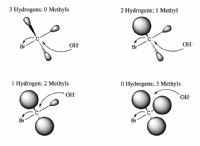
その理由は次のとおりです。
* 酸素は非常に感動的です: これは、電子を引き付ける傾向が強いことを意味します。
* ほとんどの化合物では、酸素は2つの共有結合を形成します: これらの結合は極性であり、酸素原子は電子密度をそれ自体に引っ張っています。これにより、酸素原子の部分的な負電荷が生じます。
* 酸化状態は仮想電荷を表します: -2の酸化状態は、酸素原子のこの部分的な負電荷を表します。
例外:
* 過酸化物(過酸化水素、h₂o₂など)では、酸素の酸化状態は-1。 これは、2つの酸素原子が電子を等しく共有しているためです。
* スーパーオキシド(スーパーオキシドカリウム、KO₂など)では、酸素の酸化状態は-1/2。 これは、これらの化合物の異常な結合構造によるものです。
* フッ素を含む化合物では、酸素は正の酸化状態を持つことができます。 フッ素は最も電気陰性の要素であるため、酸素から電子を引き離すことができます。
ただし、-2酸化状態が最も一般的であり、特に信じる特定の理由がない限り想定されることを覚えておくことが重要です。