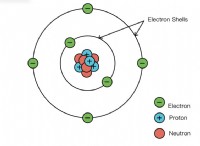
* ナトリウム(Na) 安定した電子構成を実現するために1つの電子を簡単に失う高度に反応性のある金属です。
* 塩素(cl) 安定した電子構成を実現するために1つの電子を容易に獲得する高反応性の非金属です。
*ナトリウムと塩素が反応すると、ナトリウムはその電子を塩素に *寄付 *し、正に帯電したナトリウムイオン(Na+)と負に帯電した塩化物イオン(Cl-)を形成します。
*これらの反対に帯電したイオンは、静電力を通して互いに引き付けられ、イオン結合を形成します 化合物塩化ナトリウム(NaCl)の作成 、テーブルソルトとも呼ばれます。
塩の形成は非常に発熱です 反応は、それが熱と光の形でエネルギーを放出することを意味します。 これが、ナトリウムが塩素と反応するときに明るい黄色の炎を見る理由です。
これが概要です:
ナトリウム +塩素→塩化ナトリウム(塩)
Na + Cl→NaCl