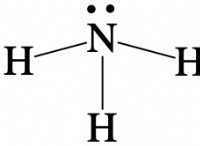
* 硝酸(hno₃)は強力な酸化剤です。 これは、他の物質から電子を容易に受け入れ、それらを酸化することを意味します。
* 水素(H₂)は還元剤です。 これは、容易に電子を寄付し、他の物質を減らすことを意味します。
硝酸が金属と反応すると、それは主に水素ガスではなく窒素の酸化物(no₂またはnoなど)を形成します。 硝酸は金属を酸化し、それ自体がその過程で減少します。
簡単な例:
* 硝酸と銅の反応:
*4hno₃(aq) + cu(s)→cu(no₃)₂(aq) +2no₂(g) +2h₂o(l)
hno₃の代わりに、希釈硫酸(h₂So₄)や塩酸(HCl)などの酸化酸を使用して水素ガスを生成します。
ここに、水素ガスを調製するための典型的な反応があります:
* 亜鉛硫酸と亜鉛の反応:
* Zn(s) +h₂so₄(aq)→znso₄(aq) +h₂(g)
他に質問がある場合はお知らせください!