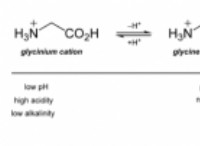
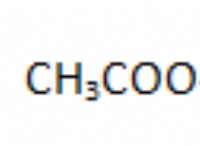酸の定義を理解する
* arrhenius酸: 水に溶解すると、H+イオン(陽子)を生成します。
* brønsted-lowry酸: 化学反応でプロトン(H+)を寄付します。
オプションの分析
* a。 PO43-(リン酸イオン): プロトン(H+)を受け入れることができるため、これはベースです。
* b。 HCl(塩酸): これは、ArrheniusとBrønsted-Lowry酸の両方です。水中でH+イオンを生成し、反応でプロトンを寄付します。
* c。 NH4+(アンモニウムイオン): これは、プロトンを寄付できるため、Bronsted-Lowry酸です。 ただし、水に溶解したときにH+イオンを生成しないため、アレニウス酸ではありません。
* d。 BF3(トリフルオリドホウ素): これはルイス酸(電子ペアを受け入れる)ですが、寄付するプロトンがないため、Brønsted-Lowry酸ではありません。
答え
正解は cです。 NH4+(アンモニウムイオン) 。
それはプロトンを寄付できるが、水中でH+イオンを生成しないため、Bronsted-Lowry酸であるため、アレニウス酸ではありません。