1。 共有結合: 酸素は、2つの水素原子と共有結合を形成して、水分子(H₂O)を形成します。これは、彼らが電子を共有し、強く安定した結合を生み出すことを意味します。
2。 極性: 電子の不均一な共有により、水分子の酸素原子はわずかに負の電荷を持ち、水素原子はわずかに正電荷を持っています。これにより、水は極性分子になります。つまり、正と負の端があります。
3。 水素結合: 水分子の極性により、互いに水素結合を形成することができます。これらは、1つの分子のわずかに陽性の水素原子と別の分子のわずかに負の酸素原子との間の弱い結合です。これらの水素結合は、水のユニークな特性の多くを担当しています。
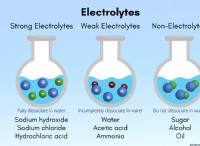
4。 溶解度: 水は、その極性により他の極性分子と相互作用できるため、溶媒が良好です。これが、塩や砂糖を含む多くの物質が水に溶ける理由です。
5。 反応: 水中の酸素は化学反応に関与する可能性があります。たとえば、光合成中に発生したものなど、酸化還元反応に関与する可能性があります。
6。 溶解酸素: 酸素は水の成分ですが、水は遊離酸素原子を含んでいません。代わりに、溶存酸素が含まれています。これは、大気から水に溶解した酸素ガス(O₂)です。この溶存酸素は、呼吸に使用するため、水生寿命に不可欠です。
7。 温度と溶解度: 水中の溶解酸素の溶解度は、温度の上昇とともに減少します。これが、冷たい水に暖かい水よりも溶解した酸素が含まれている理由です。
要約すると、水中の酸素は単なるパッシブ成分ではありません。結合、極性の作成、水素結合の形成に積極的に参加します。これらの特性は、水のユニークな特性につながり、地球上の生活に不可欠になります。