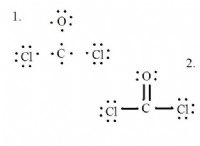* 共有結合: これらは分子内で最も強い結合であり、原子を一緒に保持します。それらは、分子のすべての炭素、水素、酸素原子の間に見られます。
* 水素結合: これらは、カルボキシル基(COOH)の電気陰性酸素原子と分子の他の部分の水素原子の間に発生する弱い結合です。これらの水素結合は、水への溶解度など、クエン酸の構造と特性に役割を果たします。
これが個々の債券の内訳です:
* C-C結合: 炭素原子間の単一共有結合。
* C-H結合: 炭素と水素原子の間の単一共有結合。
* c-o結合: 炭素と酸素原子の間の単一および二重共有結合。
* o-H結合: 酸素と水素原子の間の単一共有結合。
クエン酸にはイオン結合はありませんが、そのカルボキシル基は水で解離し、水素イオン(H+)を放出し、クエン酸イオンを形成できます。この解離プロセスは、クエン酸の酸性の性質に関与しています。