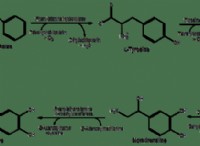
* 電気陰性度: 硫黄(S)とフッ素(F)はどちらも非金属です。 フッ素は最も電気陰性の要素であり、電子に強い魅力を持っていることを意味します。硫黄とフッ素の電気陰性度の違いは、極性結合結合を作成するのに十分な大きさですが、イオン結合を形成するほど大きくはありません。
* 結合自然: 共有化合物では、原子は電子を共有して安定した電子構成を実現します。 SF3では、硫黄原子は3つのフッ素原子と電子を共有して、3つの共有結合を形成します。
* 構造: SF3にはピラミッド型の形状があり、これは中心原子に電子の孤立ペアを持つ共有共有化合物の特徴です。
要約する: SF3は、硫黄とフッ素原子の間の電子の共有により、極性共有結合の形成につながるため、共有化合物です。