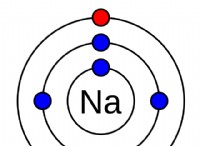
* イオン結合 金属と非金属の間に形成されます。 金属原子は電子を失い、正の帯電イオン(陽イオン)になり、非金属原子は電子をゲインして負に帯電したイオン(アニオン)になります。これらの反対に帯電したイオンは、互いに引き付けられ、結合を形成します。
* 共有結合 2つの非金属の間に形成されます。原子は電子を共有して、安定した電子構成を実現します。
水中では、水素(H)と酸素(O)の両方が非金属です。酸素は、水素よりも高い電気陰性度(電子のその引力は強い)を持っています。これは、H-O結合内の共有電子が酸素原子に近いことが見られる可能性が高いことを意味します。真のイオン結合ではありませんが、この電子の不均等な共有は水分子にわずかな極性を与え、極性共有分子になります 。
共有結合や水の極性についてもっと知りたい場合はお知らせください!