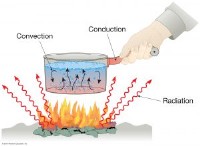
* 債券の破壊にはエネルギーが必要です: 化学結合はエネルギーを保存します。絆を破るには、エネルギーを供給する必要があります。このエネルギーは、多くの場合、熱、光、または電気エネルギーとして供給されます。
* 結合形成はエネルギーを放出します: 新しい債券が形成されると、エネルギーが解放されます。このリリースは、熱、光、さらには音の形である可能性があります。
正味のエネルギーの変化:
化学反応の全体的なエネルギーの変化は、反応物の結合を破るために必要なエネルギーと、製品に新しい結合が形成されたときに放出されるエネルギーの違いに依存します。
* 吸熱反応: 新しい結合が形成されたときに放出されるよりも多くのエネルギーが結合を破るのに必要な場合、反応は周囲からのエネルギーを吸収します。これは吸熱反応です。
* 発熱反応: 結合を破るために必要な新しい結合が形成されたときにエネルギーが放出される場合、反応は周囲にエネルギーを放出します。これは発熱反応です。
結論:
すべての化学反応には、化学結合の破壊と形成が含まれ、このプロセスは必然的にエネルギーの変化につながり、周囲からエネルギーを吸収するか、エネルギーをそれらに放出します。