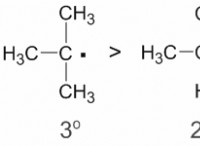
これが故障です:
* 電気陰性度: 化学結合の一部である場合、電子を自分自身に引き付ける原子の能力の尺度。
* 化学結合: 分子に原子を一緒に保持する力。
* 電子: 原子の核を周回する負に帯電した粒子。
電気陰性度に影響する要因:
* 核電荷: 核内のより多くのプロトンは、電子をより強く引き付けます。
* 原子半径: 電子が核に近いため、小さい原子は電子をより強く引っ張っています。
* 電子シェルの数: 電子殻が少ない原子は、電子をより強く引っ張っています。
電気陰性度と結合:
電気陰性度は、原子間の結合のタイプを決定する上で重要な役割を果たします。
* 非極性共有結合: 2つの原子が類似した電気陰性度を持つ場合、電子を均等に共有します。
* 極性共有結合: 2つの原子の電気陰性度が異なると、より電気陰性の原子がより強く共有電子をより強く引き付け、その原子に部分的な負電荷と他の原子に部分的な正電荷を生成します。
* イオン結合: 2つの原子間の電気陰性度の違いが非常に大きい場合、電気陰性の原子がより多くの電子をより少ない電気原子から完全に採取し、互いに引き付ける反対の電荷を持つイオンを作成します。
電気陰性度を理解するのに役立ちます:
*分子の極性
*化合物の反応性
*形成された化学結合の種類
*材料の特性
他に質問がある場合はお知らせください!