その理由は次のとおりです。
* brønsted-lowry定義: 酸の最も一般的な定義は、Brønsted-Lowryの定義です。この定義では、酸はプロトン(H+)を寄付する物質であると述べています。
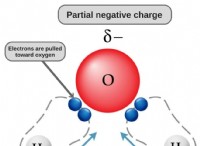
* 水: 酸が水に溶解すると、水素イオン(H+)を溶液に放出します。これが溶液を酸性にするものです。
例えば:
* 塩酸(HCl): HCl→H + + cl-
* 硝酸(HNO3): HNO3→H + + no3-
水素イオンは酸の決定的な特性であるが、水素を含むすべての物質が酸ではないことに注意することが重要です。たとえば、水(H2O)には水素が含まれていますが、酸性ではありません。