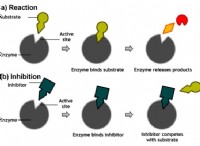
* 分子構造: CO2は、中心に炭素原子と2つの酸素原子を結合した線形分子です。この構造は対称的で非極性です。
* 分子間力の弱い: CO2の非極性の性質により、存在する主要な分子間力は、ロンドン分散力が弱いことです。これらの力は一時的であり、分子周辺の電子分布の変動から生じます。
* 低分子量: CO2の分子量は比較的低い(44 g/mol)。これは、分子が軽量であり、自由に動くことができることを意味します。
なぜこれがガス状の状態につながるのか:
* 弱い力と低分子量: 弱い分子間力と低分子量により、CO2分子はそれらの間の引力を克服し、通常の温度と圧力で気体状態で自由に移動することができます。
* 熱エネルギー: 室温では、CO2分子の熱エネルギーは、弱いロンドン分散勢力を克服するのに十分であり、独立して動き回ることができます。
その他の要因:
* 圧力: より高い圧力では、CO2分子は互いに近づき、ロンドン分散勢力の強度を高めます。これにより、CO2の液体状態への凝縮につながる可能性があります。
* 温度: 低温では、CO2分子の熱エネルギーが減少します。これにより、それらの間の引力を克服する能力が低下し、CO2は液体状態に凝縮できます。
要約: 非極性の線形分子構造、弱い分子間力、および低分子量の組み合わせにより、CO2は標準温度と圧力でCO2をガスにします。