固体状態のイオン化合物:
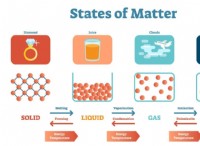
* 格子構造を修正: 固体状態では、イオン化合物は硬い結晶格子として存在します。イオンは、強い静電力によってその位置にしっかりと保持されます。
* 無料電荷キャリアなし: イオンは所定の位置にロックされており、自由に動くことはできません。このモバイル電荷キャリアの欠如は、固体化合物が電気を導入できないことを意味します。
溶融状態または溶解状態のイオン化合物:
* モバイルイオン: イオン化合物が水に溶けたり溶けたりすると、硬い格子構造が崩壊します。
* 融解: 熱エネルギーは静電力を克服し、イオンが自由に移動できるようにします。
* 溶解: 極水分子はイオンを囲み、静電魅力を弱め、イオンが独立して分離して移動できるようにします。
* 無料電荷キャリア: イオンは、液体または溶液全体で自由に移動できるようになりました。これらのモバイルイオンは電荷キャリアとして機能し、物質が電気を導入できるようにします。
キーポイント:
* 電解質: 溶けたり溶けたりしたときに電気を伝導するイオン化合物は、電解質と呼ばれます。
* 強い電解質と弱い電解質: 導電率の程度は、化合物がイオンに溶解または解離する程度に依存します。強い電解質は完全に溶解しますが、弱い電解質は部分的にしか解離しません。
要約:
イオン化合物の電気伝導率の変化は、イオンの可動性の変化によるものです。 固体状態では、イオンは固定されており、電気を導入できません。しかし、溶けたり溶けたりすると、自由に移動できるようになり、物質が電気を伝達できるようになります。