1。イオンを特定します:
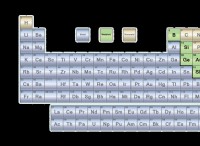
* 金属: 金属は陽イオン(正のイオン)を形成します。その充電は通常、周期表のグループ番号から予測可能です。たとえば、グループ1金属は+1イオンを形成し、グループ2金属は+2イオンを形成します。 一部の金属には複数の可能な電荷(鉄、Feなど)があるため、電荷を示すために名前でローマ数字を使用する必要があります。
* 多原子イオン: これらは、全体的な電荷を持つ原子のグループです。一般的な多原子イオンを暗記するか、チャートにアクセスできる必要があります。
2。料金を決定します:
* 金属: 存在する場合はローマ数字を使用するか、周期表のグループに基づいて電荷を推定します。
* 多原子イオン: 記憶されたリストまたはチャートから料金を使用します。
3。料金のバランス:
*陽イオンとアニオンの電荷はゼロまでバランスを取る必要があります。
* 料金がすでにバランスが取れている場合: 最初に金属記号を書き、次にポリ原子イオンシンボルが続きます。複数の原子がある場合、括弧内に多原子イオンを囲みます。
* 料金がバランスが取れていない場合: 料金の最も一般的な倍数(LCM)を見つけます。 LCMを使用して、各イオンのサブスクリプトを決定して、電荷を等しく反対にします。
例:
リン酸カルシウムの式を書きたいとしましょう 。
* カルシウム(CA): グループ2金属、そのため、その電荷は+2です。
* リン酸(po₄): -3の電荷を持つ多原子イオン。
* バランス:
* 2と3のLCMは6です。
*カルシウムから+6を取得するには、3つのCaイオン(3 x +2 =+6)が必要です。
*リン酸塩から-6を取得するには、2つのポアイオン(2 x -3 =-6)が必要です。
* 式: ca₃(po₄)
追加メモ:
* プレフィックス: 三元イオン化合物は、「モノ」、「di-」などのプレフィックスを使用しません。
* ストックシステム: ローマの数字は、いくつかの命名システム(ストックシステム)で金属の電荷を示すために使用されます。
* 一般的な多原子イオン: 一般的な多原子イオンを覚えておくか、チャートを手元に置いてください。いくつかの例は次のとおりです。
*硝酸(いいえ)
*硫酸塩(so₄²⁻)
*炭酸塩(co₃²⁻)
*水酸化物(ああ)
*アンモニウム(nh₄⁺)
練習は重要です! これらの化合物を使用すればするほど、名前から式を書きやすくなります。