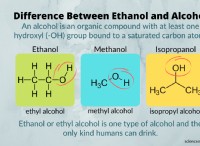
* 水素結合: エタノール(CH3CH2OH)には、水素結合を可能にするヒドロキシル基(-OH)があります。 水素結合は、水素原子が酸素のような非常に感動性のある原子に引き付けられる強力な分子間力です。この魅力は、エタノール分子間の強い結合を形成し、それらを破壊し、分子間力を克服するためにより多くのエネルギーを必要とします。
* van der Waals Force: ジエチルエーテル(CH3CH2OCH2CH3)には、ヒドロキシル基がありません。したがって、分子間に弱いファンデルワールス力を形成することしかできません。これらの力は水素結合よりも弱く、壊れるエネルギーが少ないため、沸点が低くなります。
要約:
* エタノール: 強い水素結合は、より高い沸点につながります。
* ジエチルエーテル: より弱いファンデルワールスの力は、沸点が低くなります。
したがって、エタノールは、エタノール中の分子間力(水素結合)が存在するため、ジエチルエーテルよりも著しく高い沸点を持っています。