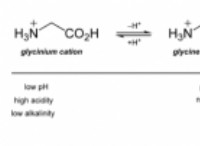
その理由は次のとおりです。
* 溶解度: CDSは比較的不溶性硫化物であり、水に容易に溶解しないことを意味します。
* 酸性条件: 酸性溶液では、硫化物イオン(s²⁻)をプロトン化して硫化水素(H₂S)を形成します。これは弱酸です。この反応は、平衡を溶解した型のCDにシフトし、降水を防ぎます。
* 溶液の希釈: 酸性溶液が希釈されると、H⁺イオンの濃度が減少します。これにより、平衡がs²⁻イオンの形成に向かって戻ってシフトし、CDの沈殿につながります。
キーポイント: 金属硫化物の溶解度はpHに依存しています。酸性条件では、ほとんどの硫化物は溶解したままであり、中性またはアルカリ性の状態では、沈殿する可能性が高くなります。