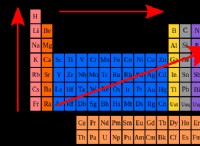
* カリウム(k) グループ1(アルカリ金属)の金属であり、安定した電子構成を実現するために1つの電子を容易に失います。それは正に帯電したイオン(K+)になります。
* 臭素(BR) グループ17(ハロゲン)の非金属であり、安定した電子構成を実現するために1つの電子を容易に獲得します。負に帯電したイオン(BR-)になります。
正に帯電したカリウムイオン(K+)と負に帯電した臭化物イオン(BR-)の間の静電引力は、イオン結合を形成します。これにより、イオン化合物臭化カリウム(KBR)が形成されます 。