1。ルイス構造:
* 窒素(n): 5価電子
* 酸素(O): それぞれ6価電子
* チャージ: +1(イオンの-1電荷から)
総価電子電子=(5 + 6 * 3) + 1 =24
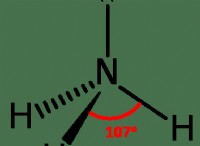
硝酸塩のルイス構造は次のように見えます:
o
/ \
いいえ
\ /
o
* 二重結合: 窒素と2つの酸素の間には2つの二重結合があります。
* 単一結合: 窒素と残りの酸素の間には1つの結合が1つあります。
2。 SigmaおよびPi結合:
* sigma(σ)結合: Sigma結合は、核軸に沿った原子軌道の直接的なオーバーラップによって形成されます。すべての1つのダブルボンドには、1つのシグマボンドがあります。
* pi(π)結合: PI結合は、原子軌道の並べ替えによって形成されます。各二重結合には、1つのシグマボンドと1つのPI結合があります。
3。シグマボンドのカウント:
* 3つのがあります シグマ結合硝酸塩は、単一結合と二重結合のそれぞれに1つ。
したがって、硝酸イオンには3つのシグマ結合があります。