* ガスは非常に圧縮可能です: ガスは非常に弱い分子間力を持ち、分子が広がり、占有するスペースを埋めることができます。
* ガスにはランダムな動きがあります: ガス分子は絶えず動き、ランダムな方向に移動します。この動きにより、容器全体に混ざり合い、均等に分配できます。
これがあなたが見ることができるものです:
* 容器内の総圧力が増加します: ガスの圧力は、容器の壁と衝突する分子の数に関連しています。 2つのガスが混合されると、より多くの分子が存在するため、より多くの衝突と全体的な圧力が高くなります。
* 各ガスの部分的な圧力は一定のままです: 各ガスは、その部分的な圧力として知られる独自の圧力を発揮します。これは、他のガスの存在にもかかわらず変化しません。総圧力は、各ガスの部分圧の合計です。
例:
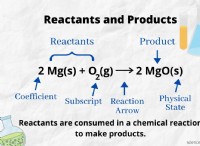
酸素ガス(O2)と窒素ガス(N2)を同じ容器に配置することを想像してください。これらの2つのガスは互いに反応しません。しばらくすると、ガスは均一に混合され、両方とも容器の全容積を占有します。 両方のガスの圧力が組み合わされているため、容器内の圧力が増加します。
注: 混合プロセスは、温度や各ガスの初期濃度などの要因の影響を受ける可能性があります。ただし、基本原理は同じままです。非反応性ガスは均一に混合し、容器の全容積を占有します。