モル濃度は、溶液中の溶質の濃度の尺度です。このモル濃度の例の問題は、溶質の量と溶液の望ましい体積が与えられた場合に、溶液のモル濃度を計算するために必要な手順を示しています。
問題
7.62 グラムの MgCl2 を注いで作成した溶液のモル濃度を計算します 400 mL の溶液を作るのに十分な量の水に入れます。
解決策
モル濃度を計算する式は

この場合、溶質は 7.62 グラムの MgCl2 です。 .式にはモル数が必要です。
周期表を使って、MgCl2 の分子量を 95.21 グラム/モルです。 MgCl2 中の 7.62 グラムのモル数を求めてください .
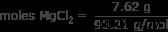
モル MgCl2 =0.08モル
モル濃度もリットル単位である必要がありますが、ではありません ミリリットル。
ソリューションの最終容量は 400 mL、つまり 0.4 L です。
この情報を式に当てはめます

M =0.2 mol/L または 0.2 M
答え
MgCl2の濃度