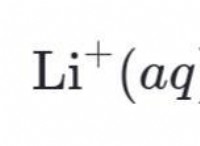その理由は次のとおりです。
* 強酸は水で完全に解離します。 これは、彼らが完全にイオンに分解されることを意味します。
* 酸の定義特性は、水に溶解したときに水素イオン(H+)を放出することです。
* 水酸化物イオン(OH-)は塩基の特徴です。 水自体には自己固有化のためにH+とOHIONの両方が少ないが、強酸の存在は圧倒的にバランスを水素イオンにシフトします。
例:
塩酸(HCl)は強酸です。水に溶けると、H+とcl-イオンに完全に解離します。
hcl(aq)→h +(aq) + cl-(aq)
この溶液は、H+イオンの高濃度と非常に低濃度のOHイオンを持ちます。
要約すると、強酸は、水酸化物イオンではなく、溶液中に大量の水素イオンを生成する能力によって定義されます。