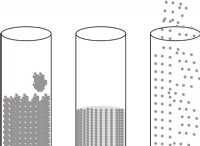
その理由は次のとおりです。
* 強酸 溶液中に完全に解離し、H+イオンを放出します。
* 強いベース 溶液中に完全に解離し、オハイオンを放出します。
*強酸と強いベースが反応すると、互いに中和し、水(H2O)と塩を形成します。
*塩は、塩基からの陽イオンと酸からの陰イオンで構成されています。
*強酸と塩基から形成されたこれらのイオンは、水と反応してH+またはOHIONIONを生成するため、pHに影響しません。
ニュートラルイオンの例:
* na+およびcl-: NaOH(強いベース)とHCl(強酸)の反応から形成されました
* k+およびno3-: KOH(強いベース)とHNO3(強酸)の反応から形成された
* Ba2+およびSO42-: BA(OH)2(強いベース)とH2SO4(強酸)の反応から形成されました
重要な注意:
*弱酸または弱い塩基から形成されたイオン意志 溶液のpHに影響します。これは、弱酸と塩基が部分的にしか解離しないため、水と反応してH+またはOHIONIONを生成できる溶液中のいくつかの非関連分子が残っているためです。