1。 ch₃clの構造を理解します
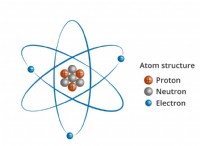
* 中央炭素原子: 炭素(c)は、ch₃clの中心原子です。
* 4つの結合ペア: 炭素は4つの単一結合を形成します:
*水素原子との3つの結合(H)
*塩素原子(CL)との1つの結合
2。価電子シェル電子ペア反発(VSEPR)理論
* 電子ドメイン: 各結合(シングル、ダブル、またはトリプル)は、中央原子の周りの電子ドメインを表します。 Ch₃Clには、4つの電子ドメインがあります。
* 反発の最小化: VSEPR理論は、中央原子の周りの電子ドメインがそれらの間の反発を最小限に抑えるために自分自身を整えると述べています。これは、特定の幾何学的な形状につながります。
3。四面体の形状
* 4つの電子ドメイン: Ch₃Clでは、炭素原子の周りの4つの電子ドメイン(4つの単一結合)が四面体形状に並んでいます。
* 結合角: 四面体の結合角は約109.5°です。これは、水素原子と塩素原子が三角形のベースを持つピラミッドに似た3次元形状で配置されることを意味します。
要約:
Ch₃CLは、中央の炭素原子に4つの電子ドメイン(4つの単一結合)があるため、四面体の形状を持っています。これは、109.5°に近い結合角を持つ四面体幾何学につながります。