これがバランスの取れた化学式です:
nh₃(g) + hcl(aq)→nh₄cl(aq)
これが反応中に起こることです:
* アンモニア(nh₃) 、弱いベースは、陽子受容体として機能します。
* 塩酸(HCl) 、強酸は、陽子ドナーとして機能します。
* 水素イオン(H⁺) HClからアンモニア分子(nh₃)と組み合わせる アンモニウムイオン(nh₄⁺)を形成します 。
* 塩化物イオン(Cl⁻) HClから溶液を維持し、アンモニウムイオン(nh₄⁺)と組み合わせて 塩化アンモニウム(nh₄cl)を形成します 。
観測:
*反応は発熱性であり、熱を放出します。反応混合物が暖かくなっているのを観察するかもしれません。
*閉じた容器で反応が行われると、塩化アンモニウムの白い煙が形成されるのが見えるかもしれません。
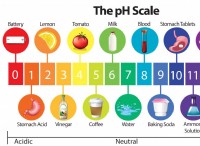
*反応が溶液中に実行されると、溶液のpHが減少し、より酸性になります。
塩化アンモニウムの使用:
*肥料
*食品添加物
*電気めっき
*メタルクリーニング
*医薬品
他に質問がある場合はお知らせください!