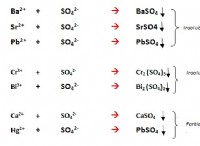
これが故障です:
* 溶質: 溶解している物質(たとえば、水中の砂糖)。
* 溶媒: 溶質(水)を溶かす物質。
* ほくろ: 物質の量の測定単位。
式:
モルリティ(M)=溶質のモル /溶媒のキログラム
単位:
モル性は通常、キログラムあたりのモル(mol/kg)で発現します 。
なぜmolalityを使用しますか?
Molalityは有用な濃度単位です。
* 温度に依存しない: 体積に基づいたモル濃度とは異なり、Molalityは温度変化とともに変化しません。
* 可変ボリュームを持つソリューションに役立ちます: Molalityは、温度や圧力のために体積が変化する可能性があるソリューションに役立ちます。
例:
2 kgの水に溶解した0.5モルのグルコースを含む溶液があるとしましょう。このソリューションのモルリリティは次のとおりです。
Molality =0.5 Moles / 2 kg =0.25 mol / kg
覚えておくべきキーポイント:
*モルリアルは濃度の尺度です。
*溶媒1キログラムあたりの溶質のモルとして定義されます。
*温度から独立しています。
*さまざまなボリュームを備えたソリューションに役立ちます。