これが故障です:
重要な機能:
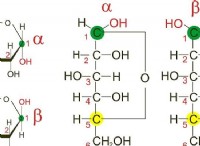
* 中央原子: 四面体の中心には、単一の原子があります。
* 4つの結合: この中心原子は、他の原子または原子グループと4つの結合を形成します。
* 結合角: 任意の2つの結合間の角度は約109.5度です。
* 対称性: 四面体の形状は4つの等しい面を持ち、それぞれ三角形で、非常に対称的です。
四面体分子の例:
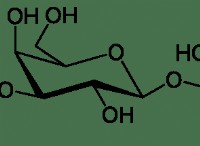
* メタン(CH4): メタン中の炭素原子は、4つの水素原子に結合されています。
* 水(H2O): 水は全体的に曲がっていますが、その中心酸素原子は水素原子と2つの孤立した電子ペアに2つの結合を形成し、酸素の周りに四面体の配置をもたらします。
* アンモニウムイオン(NH4+): 窒素原子は4つの水素原子に結合します。
四面体形状の重要性:
* 結合: 四面体の形状により、結合された原子または原子基の最大分離が可能になり、電子電子反発が減少し、安定性が最大化されます。
* 反応性: 分子の形状は、他の分子と相互作用する方法を指示するため、その反応性に影響を与える可能性があります。
* 物理的特性: 四面体分子は、しばしば融点、沸点、溶解度などのユニークな特性を示します。
四面体構造の識別:
* vsepr理論: この理論は、中心原子を囲む電子ペアの数に基づいて分子の形状を予測します。中央原子の周りの4つの電子ペアは、一般に四面体幾何学をもたらします。
* 分子モデル: 物理モデルの構築は、分子内の原子の3次元配置を視覚化するのに役立ちます。
注: 多くの分子は四面体構造を採用していますが、電子の孤立ペア、結合長、分子間力などの要因のために例外があります。