燃焼:
*木材、プロパン、天然ガス、ガソリンなどの燃焼燃料。これは、発熱反応の最も一般的な例です。
*可燃性物質の燃焼(紙、エタノールなど)。
中和反応:
*強酸(HCLなど)と強い塩基(NAOHなど)を混合します。反応は熱を生成し、塩と水を形成します。
爆発:
*ダイナマイトやTNTなどの爆発物の急速な燃焼。これらの反応は、短時間で膨大な量のエネルギーを放出します。
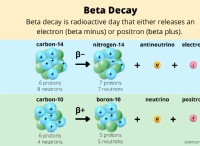
核反応:
*核核分裂、原子の核が2つ以上の軽い核に分割されます。これは、原子力発電所で使用されるプロセスです。
*核融合。2つ以上の原子核が結合して、1つ以上の異なる原子核と亜原子粒子(中性子または陽子)を形成します。これが星を動かすプロセスです。
その他の例:
* 鉄の錆び: 酸素と水の存在下での鉄の酸化は、ゆっくりと熱を放出します。
* 濃縮酸の溶解: 濃縮硫酸(h₂SO₄)または硝酸(HNO₃)と水を混合すると、かなりの熱が放出されます。
* ナトリウムと水の間の反応: これにより、水素ガスが生成され、熱が放出されます。
重要な注意: これらはほんの数例です。他の多くの化学反応は発熱性です。反応が発熱性であるか吸熱性であるかは、反応のエンタルピー変化(ΔH)を測定することで決定できます。発熱反応には負のΔHがあり、熱が放出されることを示しています。
他に質問がある場合はお知らせください。