これが故障です:
* 酸 溶液中の水素イオン(H+)を放出する物質です。彼らは7未満のpHを持っています。
* ベース 溶液中に水酸化物イオン(OH-)を放出する物質です。彼らは7を超えるpHを持っています。
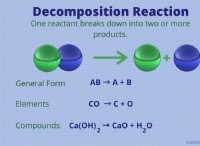
酸とベースが反応すると、それらはお互いを中和します。この反応は塩と水を形成します:
酸 +ベース→塩 +水
例えば:
* 塩酸(HCl) +水酸化ナトリウム(NAOH)→塩化ナトリウム(NaCl) +水(H₂O)
その他の重要なポイント:
*酸またはベースの強度は、他方をどれだけ容易に中和するかを決定します。強酸と塩基は互いに完全に中和します。
* pHスケールは、溶液の酸性度または塩基性を測定します。ニュートラルソリューションのpHは7です。
*中和反応は、化学物質の製造、廃水の治療、および安定したpHを維持するための人体など、多くの用途で重要です。