1。ルイス構造:
* 価電子: ヒ素(AS)には5つの原子価電子があり、塩素(Cl)には7があります。
* 総価電子電子: 5(as) + 3 * 7(cl)=26
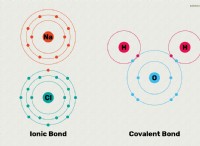
* 原子の接続: 各塩素原子は、6つの電子(各結合に2)を使用して、ヒ素原子と単一の結合を形成します。
* 残りの電子: 26-6 =20電子
* 孤立ペア: これらの残りの電子は、原子の周りに唯一のペアを形成します。 すでに6個の電子を使用しているため、残り20〜6 =14個の電子があります。 それは7つの唯一のペアです。 これらを原子に分け、3つの孤立ペア(6つの電子)と各Cl 2の孤立ペア(それぞれ4電子)として与えます。
2。 as:の孤独なペア
ルイスの構造は、ASCL3のAS原子に電子の1つの孤独なペアがあることを示しています 。
覚えておいてください: 唯一のペアは、結合に関与していない電子のペアです。