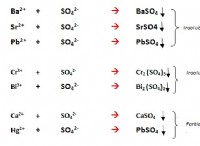
ここにいくつかの例があります:
* 水(h₂o): 水は、水酸化物イオン(OH⁻)を形成するために陽子(H⁺)を寄付することにより、酸として作用できます。また、陽子を受け入れて水素イオン(h₃o⁺)を形成することにより、塩基として作用することもできます。
* 重炭酸塩イオン(HCO₃⁻): 炭酸塩を形成するためにプロトンを寄付するか(Co₃²⁻)、酸素酸(H₂Co₃)を形成するプロトンを受け入れることができます。
* アミノ酸: 酸性カルボキシル基(-COOH)と塩基性アミノ基(-NH₂)の両方を持っています。
* 金属水酸化物: 水酸化アルミニウム(Al(OH)₃)や水酸化亜鉛(Zn(OH)₂)などの多くの金属水酸化物は両性です。それらは、酸と水を形成するために酸と反応することができ、塩基で複合イオンを形成することができます。
両性物質の重要な特徴は、条件に応じて陽子を寄付または受け入れる能力です。