その理由は次のとおりです。
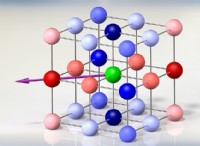
* イオン結合 1つの原子(通常は金属)が電子を失い、正に帯電した陽イオンになると形成され、別の原子(通常は非金属)がこれらの電子を獲得して負に帯電した陰イオンになります。この電子移動により、両方の原子が電子の完全な外側の殻を持ち、オクテットルールを満たし、安定性を達成します。
* 共有結合 2つの原子が電子を共有するときに形成します。電子を共有することにより、両方の原子が電子の完全な外殻を実現し、オクテットのルールを満たし、安定性を達成します。
したがって、メカニズムは異なっていますが、イオン結合と共有結合の両方が、関与した原子の安定した電子構成につながり、より安定した分子または化合物をもたらします。