その理由は次のとおりです。
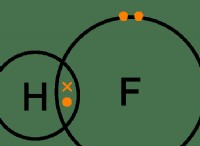
* 極性: 水分子は極性です。つまり、わずかに正の端(水素原子)とわずかに負の端(酸素原子)があります。これは、酸素が水素よりも電気陰性であり、共有電子をより強く引き付けるためです。
* 水素結合: 1つの水分子のわずかに正の水素原子は、別の水分子のわずかに負の酸素原子に引き付けられます。この魅力は水素結合と呼ばれます。
これらの水素結合は、水分子自体内の共有結合と比較して比較的弱いです。しかし、それらは水分子を一緒に保持するのに十分な強さであり、水に次のようなユニークな特性を与えます。
* 高沸点: 水素結合を壊すために必要なエネルギーのため、水は予想よりも高い沸点を持っています。
* 高い表面張力: 表面の水分子は、空気よりも強く互いに引き付けられ、表面張力が生じます。
* 良い溶媒: 水の極性により、多くの物質を溶解することができ、優れた溶媒になります。
したがって、水素結合は、水分子間の引力の原因となる重要な特性です。