1。好ましい格子エネルギー:
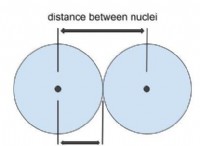
*反対の電荷のイオンが一緒になると、それらの間に静電魅力が存在します。このアトラクションは、格子エネルギーによって定量化されます 、これは、1モルのイオン固体がその気体イオンから形成されたときに放出されるエネルギーです。
* より高い格子エネルギー イオン間のより強い魅力を示し、固体格子の形成がより有利になっていることを示します。
2。低溶解度製品(ksp):
* 溶解性製品(ksp) は、控えめに溶けやすいイオン化合物が水に溶ける程度の尺度です。化合物の溶解の平衡定数を表します。
* 低ksp 値は、固体化合物が比較的不溶性であり、イオン濃度の生成物がKSP値を超えると溶液から沈殿することを示しています。
3。エントロピーの考慮事項:
*固体沈殿物の形成はシステムのエントロピーを減少させますが(障害が少ない)、周囲の水分子のエントロピーの増加により、全体的なエントロピーの変化はしばしば好ましいです。
*イオンが結合して固体を形成すると、以前に潤いを与えていた水分子が放出されます。これらの解放された水分子は、より自由に移動できるようになり、溶液のエントロピーが増加するようになりました。
要約:
*イオンの組み合わせが格子エネルギーが高く、溶解度が低い固体化合物につながると、沈殿物の形成が良好になります。
*全体的なエントロピーの変化は、溶媒のエントロピーの増加により降水量を支持することが多いため、プロセスをさらに強化します。
例:
* 塩化銀(AGCL): AGCLのKSPは非常に低いため、非常に不溶です。銀イオン(Ag+)と塩化物イオン(Cl-)が溶液中に出会うと、イオンとAgClの低溶解度の間の強い静電引力のために、それらは容易に沈殿物を形成します。
* 硫酸バリウム(BASO4): また、BASO4にはKSPが低く、不溶性です。溶液中のバリウムイオン(BA2+)と硫酸イオン(SO42-)の混合は、BASO4の白色沈殿物の形成につながります。
温度、pH、他のイオンの存在などの要因がイオン化合物の溶解度、したがって沈殿物の形成に影響を与える可能性があることに注意することが重要です。