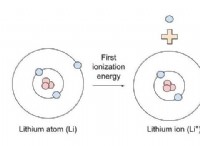
1S²2S²2p²
これがそれが意味することです:
* 1S²: 最初のエネルギーレベル(n =1)には、1つのサブシェル、「S」サブシェルがあります。このサブシェルは最大2つの電子を保持でき、両方とも炭素で満たされます。
* 2S²: 2番目のエネルギーレベル(n =2)には、2つのサブシェル、「S」と「P」サブシェルがあります。 「S」サブシェルは2つの電子で満たされています。
* 2p²: 2番目のエネルギーレベルの「P」サブシェルは最大6つの電子を保持できますが、炭素はこのサブシェルに2つの電子しかありません。
なぜこれが重要なのですか?
電子構成は、元素の化学的特性を決定します。カーボンの構成は、4つの共有結合を形成する能力につながり、私たちが知っているように、有機化学と生命の基礎となっています。