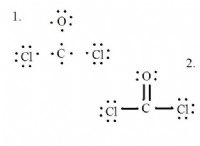その理由は次のとおりです。
* 陽子: 原子の質量に大きく寄与する正に帯電した粒子。
* 中性子: 原子の質量にも大きく貢献する中性粒子(電荷なし)。
* 電子: 核を周回するマイナス帯電粒子。質量はありますが、陽子や中性子に比べて非常に小さいため、原子の全体の質量を計算するのは一般に無視できます。
原子質量単位(AMU):
原子の質量は通常、原子質量単位(AMU)で発現します。 1つのAMUは、炭素-12原子の質量1/12として定義されています。
キーポイント:
*原子の陽子の数は、その原子数とそれが表す要素を定義します。
*原子の中性子の数は異なる場合があり、質量が異なる同じ元素の同位体を作成します。
*原子の陽子と中性子の総数は、その質量数と呼ばれます。
したがって、原子の質量は、それが含む陽子と中性子の数によって本質的に決定されます。