その理由は次のとおりです。
* 分子運動: 温度は、分子の平均運動エネルギーの尺度です。低温は分子が遅くなることを意味します。
* 衝突周波数: 化学反応を起こすには、分子は十分なエネルギーと衝突する必要があります。遅い分子の衝突が少なくなります。
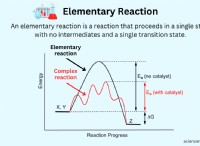
* 活性化エネルギー: すべての反応には、分子が既存の結合を破り、新しい結合を形成するために最小エネルギー(活性化エネルギー)が必要です。低温では、この障壁を克服するのに十分なエネルギーがある分子が少なくなります。
このように考えてみてください: キャンプファイヤーを始めようとしていると想像してみてください。木材が寒い場合(低温)、点火するには激しく動作する(エネルギー入力を増やす)必要があります。
例外:
これは一般的に真実ですが、例外があります。 いくつかの反応、特に熱を放出する反応(発熱)は、低温での反応物の安定性が増加するため、より低い温度で実際にわずかに速度を上げることができます。ただし、この効果は通常、反応の全体的な減速に比べて小さいです。