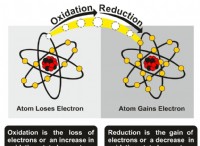
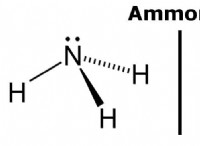
基本を理解する
* イオン化合物: これらは、金属(積極的に帯電)と非金属(負に帯電した)結合の場合に形成されます。反対に帯電したイオン間の静電引力は、化合物を一緒に保持します。
* カチオン: 正に帯電したイオン(金属)。
* アニオン: 負に帯電したイオン(非金属)。
イオン式を書くための手順
1。イオンを識別します:
*金属陽イオンと非金属陰イオンの電荷を決定します。周期表または一般的なイオンのテーブルを使用して役立ちます。
* 例: ナトリウム(Na)はA +1カチオン(Na⁺)を形成し、塩化物(Cl)はA -1アニオン(Cl⁻)を形成します。
2。料金のバランス:
*目標は、中性化合物を達成することです(ゼロの全体的な電荷)。
*料金の最も一般的な倍数(LCM)を見つけます。
* 例: na⁺とcl⁻のバランスをとるには、LCMは1です。各イオン(NaCl)の1つが必要です。
3。式を書きます:
*最初に陽イオンのシンボルを書き、次にアニオンのシンボルを書きます。
* 例: NaCl(塩化ナトリウム)
例
* 酸化マグネシウム(MGO):
*マグネシウム(mg)は+2カチオン(mg²⁺)を形成します。
*酸素(o)は-2アニオン(o²⁻)を形成します。
*料金はすでにバランスが取れているため、式はMGOです。
* 塩化アルミニウム(Alcl₃):
*アルミニウム(al)は+3陽イオン(al³⁺)を形成します。
*塩素(Cl)は-1アニオン(Cl⁻)を形成します。
*電荷のバランスをとるには、1つのアルミニウムと3つの塩素(Alcl₃)が必要です。
* 硫化カリウム(K₂S):
*カリウム(k)は+1カチオン(k⁺)を形成します。
*硫黄(S)は-2アニオン(s²⁻)を形成します。
*電荷のバランスをとるには、2つのカリウムと1つの硫黄(K₂)が必要です。
キーポイント
* subscripts: 要素記号の後に添え字として書かれた数字は、式ユニットに存在する各イオンの数を示しています。
* 括弧: ポリ原子イオン(硫酸塩など)が式に複数回表示される場合、括弧の外側のサブスクリプトと括弧内に囲まれています。
*例:リン酸カルシウム:ca₃(po₄)₂
特定のイオン化合物の書き込み式を練習したい場合はお知らせください!