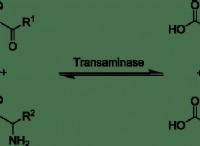
* 電気陰性の差: 酸素は炭素よりも電気陰性です。つまり、電子をより強く引き付けます。これにより、酸素原子に部分的な負電荷(Δ-)が生成され、炭素原子に部分的な正電荷(Δ+)が生成されます。
* トリプルボンド: 炭素と酸素は、1つのシグマ結合と2つのPI結合で構成されるトリプル結合を形成します。 Sigma結合は2つの原子間でより局所的になりますが、PI結合は結合軸の上下のよりも非局在化されています。
* 対称性と電子分布: 分子は線形であり、トリプル結合の電子は結合軸の周りに対称的に分布しています。この対称性は、電気陰性度の違いによって作成された個々の双極子のキャンセルにつながります。
* PI結合の極性: シグマ結合は電気陰性度の違いにより偏光されていますが、PI結合は比較的非極性です。これにより、全体的な双極子モーメントがさらに減少します。
要約:
炭素と酸素の間に電気陰性度に違いがありますが、COのトリプル結合と対称電子分布は、全体的な双極子モーメントをわずかにします。分子は、弱い極性と見なされます 。