1。価電子:
*これらは、化学結合に関与する原子の最も外側のシェルの電子です。
*原子は、安定した構成を実現するために電子を獲得、失い、または共有する傾向があり、多くの場合、ノーバーガスの電子構成に似ています(完全な外側シェルを持つ)。
2。債券の種類:
* イオン結合: ある原子が1つ以上の電子を別の原子に完全に透過すると発生します。これにより、互いに引き付ける反対の電荷でイオン(充電された原子)が作成されます。
* 例: ナトリウム(NA)には1つの価電子があり、塩素(Cl)には7つの価があります。ナトリウムは容易にその電子を失い、正の帯電イオン(Na+)になり、塩素がこの電子を獲得して負に帯電したイオン(CL-)になります。これらのイオンは互いに引き付けてイオン結合を形成します。
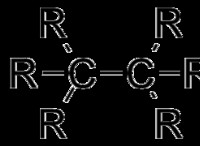
* 共有結合: 原子が電子を共有して安定した構成を実現するときに発生します。
* 例: それぞれ2つの水素原子には、1つの価電子があります。それらはこれらの電子を共有して共有結合を形成し、両方の原子が安定した充填された外殻を持つ水素分子(H2)を作成します。
* 金属結合: 電子が非局在化し、金属格子全体で自由に移動する金属原子の間で発生します。これにより、金属は導電率や順応性などの特徴的な特性を与えます。
結合に影響を与える要因:
* 電気陰性度: 原子が結合で自分自身に向かって電子を引き付ける能力。 2つの原子間の電気陰性度の差が大きいほど、結合はより多くなります。
* 原子のサイズ: より大きな原子は、核と価電子の間の弱い引力のために、より弱い結合を形成する傾向があります。
* 価電子電子の数: より多くの価電子を持つ原子は、より多くの結合を形成できます。
要約: 原子内の価電子の数と配置は、その結合挙動を決定し、イオン、共有結合、または金属結合の形成につながります。この基本的な概念を理解することは、物質の化学反応と特性を予測して説明するために重要です。