一般的なプロパティ
* 周期表の場所: 周期表の右側にある水素(H)を除き、左側に配置されています。
* 物理状態: 非金属は、室温で3つの物質状態すべてに見られます。
* ガス: 酸素(O2)、窒素(N2)、ヘリウム(HE)、ネオン(NE)、アルゴン(AR)、クリプトン(KR)、キセノン(XE)、ラドン(RN)
* 液体: 臭素(BR2)
* 固体: 炭素(C)、硫黄(S)、リン(P)、セレン(SE)、ヨウ素(I2)
* 外観: 非金属は無色、白、黄色、オレンジ、赤、茶色、または黒です。
* 導電率: 一般に、熱と電気の導体が貧弱です。
* 柔軟性と延性: 非金属は、順応性がありません(シートにハンマーできません)または延性(ワイヤに引き込むことはできません)。
* 反応性: 非金属の反応性は異なり、一部は非常に反応性があり(フッ素のように)、他のものはあまり反応性が低く(貴族のように)。
* イオンの形成: 非金属は、電子を獲得して負に帯電したイオン(アニオン)を形成する傾向があります。
化学的性質
* 酸化: 非金属は容易に電子を獲得します。これは酸化の特徴です。
* 共有結合の形成: 非金属は他の非金属と共有結合を形成し、電子を共有して安定した電子構成を実現します。
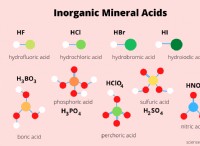
* 酸の形成: 多くの非金属は、水素(例えば、HCl-塩酸)と組み合わせると酸を形成します。
非金属とその使用の例
* 酸素(O2): 医療機器、および産業プロセスで使用される呼吸に不可欠です。
* 窒素(N2): 肥料の生産および不活性ガスアプリケーションに使用される大気に見られる。
* 炭素(c): 燃料として使用される有機化合物、鉛筆用のグラファイト、宝石用のダイヤモンドとして使用されています。
* 硫黄: 主要な工業化学物質である硫酸(H2SO4)の生産に使用されます。
* リン(P): 肥料、マッチ、花火で使用されます。
* 塩素(Cl2): 浄水と漂白剤生産で使用されます。
興味深い事実
* 貴重なガス: 周期表の最後の列にある非反応性ガス。
* ハロゲン: 周期表の最後から2番目の列に見られる高反応性非金属。
* 同種: いくつかの非金属は、同盟と呼ばれる異なる構造形態で存在します(例えば、ダイヤモンドとグラファイトは炭素の同種です)。
これは、非金属の簡単な概要です。この多様な要素のグループについて発見すべき多くの魅力的な事実と特性があります。