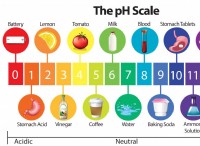
その理由は次のとおりです。
* 酸 溶液中に陽子(H+)を寄付します。
* ベース 溶液中の陽子(H+)を受け入れます。
* メタロイド 金属と非金属の両方の特性があります。それらは、酸性または溶液中の塩基として作用するイオンを容易に形成しません。
ただし、ヒ素は酸性または塩基性の可能性のある化合物を形成できます。
* ヒ素酸化物(AS2O3およびAS2O5) 酸性です。水に溶解すると、それらはそれぞれヒエノー酸(H3ASO3)とヒ素酸(H3ASO4)を形成します。
* ヒ素水素化物(ASH3) 基本です。それらは水と反応して、アルセニドイオン(AS3-)と水酸化物イオン(OH-)を形成します。
したがって、ヒ素自体は酸でも塩基でもありませんが、その化合物は、特定の化合物と水との反応に応じて酸性または塩基性の挙動を示すことができます。