その理由は次のとおりです。
* 電気陰性度: ホウ素の電気陰性度は2.04、硫黄の電気陰性度は2.58です。 電気陰性度の違いは、イオン結合を形成するのに十分な大きさではありません(通常は1.7を超える)。
* 電子の共有: ホウ素と硫黄は、安定したオクテット構成を実現するために電子を共有します。 3つの原子価電子を備えたホウ素は、3つの電子を共有する必要があり、硫黄は6つの原子価電子で2つの電子を共有する必要があります。 これは、b₂s₃のような化合物につながります。
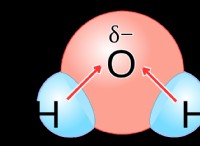
重要な注意: 結合は主に共有結合ですが、電気陰性の違いのためにわずかな極性の特性があるかもしれません。