イオン電荷:原子のバランスの取れた行為
イオン電荷は電荷です 原子または分子は、電子を獲得または失った後に運ばれます。 これが故障です:
1。原子とその部分:
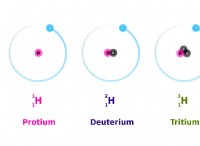
*原子は物質の基本的な構成要素です。
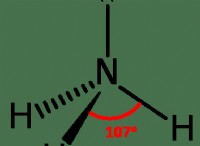
*それらは、正に帯電した核(陽子と中性子を含む)とその周りに周囲の負に帯電した電子で構成されています。
* 通常、原子には同数のプロトンと電子があり、電気的に中性になります。
2。チャージゲーム:
*原子は、電子を獲得または失う可能性があります より安定した電子構成を実現します。
* 電子の獲得: 負電荷を作成します (陽子よりも多くの電子)アニオンと呼ばれます 。
* 紛失電子: 正電荷を作成します (電子よりも多くの陽子)a cation と呼ばれます 。
3。サイズが重要:
* 電荷の大きさ: 獲得または失われた電子の数は、イオン電荷の大きさを決定します。
*たとえば、単一の電子損失は+1電荷を作成しますが、2つの電子が失われたのは+2電荷を作成します。
* 表記: イオン電荷は、SuperScript番号に続いてプラスまたはマイナスの符号で表されます。
*例:+1、-2、+3など。
4。 バランス法:
*反対の電荷を持つイオンは互いに引き付けられ、イオン結合を形成します 。
*これらの結合は、イオン化合物を生成します それは全体的に電気的にニュートラルです。
*例:ナトリウム(Na+)と塩素(Cl-)を組み合わせて、塩化ナトリウム(NaCl)、テーブル塩を形成します。
一言で言えば、イオン電荷は、電子を獲得または失った後の原子の電気的不均衡を表し、化学結合とイオン化合物の形成に重要な役割を果たします。