これが故障です:
* 電解質 水に溶けたときに電気を伝達する物質です。これは、イオン(荷電粒子)に解離するために起こります。
* イオン 電子を獲得または失った原子または分子であり、正味の正または負の電荷を与えます。
電解質の例:
* 塩: 塩化ナトリウム(NaCl)、臭化カリウム(KBR)、硫酸マグネシウム(MGSO₄)
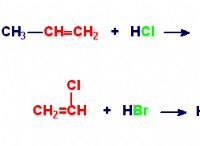
* 酸: 塩酸酸(HCl)、硫酸(H₂SO₄)、硝酸(HNO₃)
* ベース: 水酸化ナトリウム(NaOH)、水酸化カリウム(KOH)、水酸化カルシウム(CA(OH)₂)
電解質がイオンを形成する方法:
* イオン化合物: これらの化合物は、すでに固体状態(NaClなど)のイオンとして存在しています。水に溶解すると、イオンは分離し、水分子に囲まれます。
* 共有化合物: 一部の共有化合物は、水に溶解するとイオンを形成できます。たとえば、HClは水中のH⁺イオンとcl⁻イオンに分離します。
キーテイクアウト:
水に溶解したときにイオンを生成できる化合物は、電解質です。 電気を導入するこの能力は、電解質の決定的な特徴です。