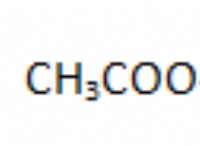* イオン結合: NaClはイオン化合物です。これは、正に帯電したナトリウムイオン(Na+)と負に帯電した塩化物イオン(CL-)の間の静電引力によって形成されることを意味します。
* 固定位置: 固体状態では、これらのイオンは硬い結晶構造に閉じ込められています。彼らは自由に動き回ることはありません。
* 無料電荷キャリアなし: 材料が電気を導入するには、自由移動する荷電粒子(電子またはイオン)が必要です。固体NaClでは、イオンは結合されており、自由に動くことはできません。
ただし、NaClが水に溶けたり溶けたりすると、電気の良い導体になります。 これは:
* 溶解: 水中では、イオン結合が壊れ、イオンは水分子に囲まれ、自由に移動できます。
* 融解: 溶けると、イオンは固定位置から解放されて動き回るのに十分なエネルギーを獲得します。
したがって、NaClが電気を導入する能力は、その物理的状態に依存します。