この化学辞書は、文字 L で始まる化学の定義を提供します。これらの用語集の用語は、化学および化学工学で一般的に使用されます。下の文字をクリックして、その文字で始まる用語と定義を見つけてください。
A B C D E F G H I J K L M N O P Q R S T U V W X Y Z
不安定な複合体 – 不安定な錯体は、周囲の溶液中の配位子と急速に平衡に達する錯イオンです。
ランタニド – 原子番号が 58 ~ 71 の元素 (ただし、ランタニドの正確な開始位置と終了位置については論争があります!).ランタニド系列は、4f サブレベルが満たされている要素のグループです。詳細については、ランタニドのセクションを参照してください。
別名:レアアースメタル、レアアースエレメント、コモンアースエレメント。
例:ユウロピウム、ランタン、ジスプロシウム、エルビウムはすべてランタニド元素です。
ランタン – ランタンは、原子番号 57 のランタニド元素の名前で、記号 La で表されます。
格子エネルギー – 格子エネルギーは、気相の反対に帯電したイオンが結合して固相のイオン格子を形成するプロセスの ΔH (エンタルピー変化) です。
格子点 – 格子点は、結晶単位セル内の原子が占める位置です。
法律 – 科学における法則とは、一連の観察結果を口頭または数学的ステートメントの形で説明するための一般化された規則です。科学的法則は、観測された要素間の因果関係を暗示しており、常に同じ条件下で適用されなければなりません。科学的法則は、観測された事象が発生する「理由」を説明しようとするのではなく、事象が実際に同じように何度も発生することのみを説明しようとします。
化学平衡の法則 – 化学平衡の法則は、平衡状態にある反応混合物には、反応物と生成物の濃度に関連する条件 (平衡定数 Kc によって与えられる) があることを示す関係です。反応 aA(g) + bB(g) ↔ cC(g) + dD(g) の場合、Kc =[ C ]·[ D ] / [ A ]·[ B ].
ボリュームの結合の法則 – 体積の結合の法則は、化学反応におけるガスの相対体積が小さい整数の比率で存在することを示す関係です (すべてのガスが同じ温度と圧力にあると仮定します)。
別名:ゲイ・リュサックの法則
例:反応中
2 H2 (g) + O2 (g) → 2 H2 O(g)
H2 2巻 1 体積の O2 と反応する 2 ボリュームの H2 を生成する O.
エネルギー保存の法則 – エネルギー保存の法則は、エネルギーを生成または破壊することはできないが、ある形から別の形に変化する可能性があると述べる法則です.
質量保存の法則 – 質量保存則は、化学反応において、生成物の質量が反応物の質量に等しいという関係です。
一定成分の法則 – 一定組成の法則は、純粋な化合物のサンプルには常に同じ元素が同じ質量比率で含まれているという化学の法則です。
別名:定比例の法則
定比例の法則 – 定比例の法則は、一定の組成の法則の別名です。上記の定義を参照してください。
倍数比例の法則 – 要素が結合すると、小さな整数の比率で結合するという法則 (同じ種類の化学結合があると仮定)。
ダルトンの法則としても知られていますが、その用語は通常、彼の分圧の法則を指します。
例:炭素と酸素が反応して CO または CO2 を形成する 、ただし CO1.6 は除く .
ローレンシウム – ローレンシウムは、原子番号 103 のアクチニド元素の名前で、記号 Lr で表されます。
リード – 鉛は原子番号 36 の金属元素の名前で、記号 Kr で表されます。
グループを脱退 – 脱離基とは、分子の残りの部分から取り除かれた原子または原子群を指します。脱離基が除去されると、その基は、以前に切断点で結合を形成した電子対を取ります。脱退グループはヌクレオフュージとも呼ばれ、一般に LG と略されます。脱離基は、プロトンからの原子の除去にも適用できます。このタイプの脱離基は、プロトンを供給した酸の共役塩基です。
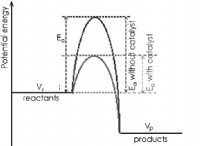
シャトリエの原則 – ルシャトリエの原理は、平衡状態にある化学系にストレスがかかると、ストレスを緩和する方向に平衡が移動する原理です。ストレスは、集中力の変化、温度の変化、圧力の変化など、多くのことを意味します。反応物が増えると平衡がシフトし、より多くの生成物が生成されます。
ルクランシュ セル – ルクランシュセルは、湿ったペーストを電解液として使用する乾電池です。
例:懐中電灯の電池はルクランシェ電池です。湿ったペースト電解質は、通常、粉末状の炭素、NH4 の組み合わせです。 Cl、MnO2 およびZnCl2 .
ライデンフロスト効果 – ライデンフロスト効果は、液体が液体の沸点よりもはるかに高温の表面に近づいたときに、液体が沸騰するのを防ぐ絶縁蒸気を生成する現象です。
例:ライデンフロスト効果の一般的な例は、非常に熱い鍋の表面を水が飛び散ることです。
レウ – Leu は、アミノ酸ロイシンの略語です。ロイシンはLとも略されます。
左旋性 – 左旋性とは、ビューアーに近づく光に対して平面偏光を反時計回りに回転させるキラル分子を指します。左旋性エナンチオマーは接頭辞 L- で示されます。
ルイス酸 – ルイス酸は、電子対受容体である物質です。
例:H は一対の電子を受け入れることができるため、ルイス酸です。ルイス塩基 OH から利用可能な電子対と結合して、H2 を形成します。 O.
ルイス酸塩基反応 – ルイス酸塩基反応は、電子対供与体 (ルイス塩基) と電子対受容体 (ルイス酸) の間に少なくとも 1 つの共有結合を形成する化学反応です。
ルイス基地 – ルイス塩基は、電子対供与体である物質です。
例:OH は、反応に供与する自由電子のペアを持っているため、ルイス塩基です。電子対をルイス酸 H に供与して、H2 を形成することができます。 O.
ルイス コンプレックス – ルイス錯体は、ルイス酸塩基反応の生成物です。ルイス酸がルイス塩基と結合すると、ルイス錯体が形成されます。
別名:ルイス酸/塩基複合体
ルイス構造 – ルイス構造は分子の構造表現であり、ドットは原子の周りの電子位置を示すために使用され、線またはドットのペアは原子間の共有結合を表します。
別名:ルイス・ドット図、電子ドット図
リガンド – 配位子は、中心原子またはイオンとの共有結合を介して 1 つまたは複数の電子を供与または共有する原子、イオン、または分子です。中心原子を安定させ、その反応性を決定するのは、配位化学における錯化基です。
リガンド フィールド分割 – 配位子場分裂は、配位子の d 軌道間のエネルギーの差です。リガンド フィールド分割数は、大文字のギリシャ文字 Δ で示されます。結晶場分裂は、2 つの類似した金属-配位子錯体間の色の違いを説明します。 Δ は酸化数とともに増加する傾向があり、周期表のグループの下に増加します。
ライトナフサ – ライトナフサは、30 °C から 60 °C で沸騰した 5 から 6 炭素の炭化水素から蒸留されたナフサの一種です。
石灰岩 – 石灰岩は、化合物の炭酸カルシウムまたは CaCO3 の結晶で構成される岩石です。 .
制限反応物 – 制限反応物は、生成される生成物の量を決定する化学反応の反応物です。
例:反応中の 1 モルの水素と 1 モルの酸素が与えられた場合:
2 H2 + O2 → 2 H2 〇
反応は水素を酸素の 2 倍の速度で消費するため、制限反応物は水素になります。
脂質 – 脂質は、脂溶性の天然分子です。
例:脂肪、油、ワックス、ステロールはすべて脂質です。
液化 – 液化は、物質をその固相または気相から液相に変換するプロセスです。
例:気体は、凝縮または冷却によって液化します。固体は加熱により液化します。
液体 – 液体は物質の状態の 1 つです。液体中の粒子は自由に流れるため、液体には一定の体積がありますが、一定の形状はありません。
例:室温:水、水銀、植物油、エタノールはすべて液相です。
リットル – リットルは体積の単位です。 1 リットルは 1000 立方センチメートルを囲むように定義されています。リットルを表すために使用される多くの記号があります:L、l、および小文字の筆記体 l (l)。最も一般的に使用される記号は大文字の L です。
別のスペル:litre
リチウム – リチウムは、原子番号 3 のアルカリ金属元素の名前で、記号 Li で表されます。
リトマス紙 – 地衣類から得られる天然の水溶性染料で処理されたろ紙。できあがった紙は「リトマス紙」と呼ばれ、pH 指示薬として使用できます。青色リトマス紙は酸性条件下 (pH 4.5 以下) で赤くなり、赤色リトマス紙はアルカリ性条件下 (pH 8.3 以上) で青色になります。中性リトマス紙は紫がかった色です。
リバモリウム – リバモリウムは、原子番号 116 の合成元素の名前で、記号 Lv で表されます。
ロンドン分散部隊 – ロンドン分散力は、互いに近接している 2 つの原子または分子間の弱い分子間力です。この力は、2 つの原子または分子が互いに接近するときに、それらの電子雲の間の電子反発によって生成される量子力です。ロンドン分散力はファン デル ワールス力の中で最も弱く、温度が下がるにつれて非極性の原子または分子が液体または固体に凝縮する力です。
別名:ロンドン力、LDF、分散力、瞬間双極子力、誘導双極子力
一組 – 孤立電子対は、原子の最外殻にある電子対で、共有も結合もされていません。
ロクス – Lox は液体酸素の略語です.
月コースティック – 月の苛性は、化合物硝酸銀または AgNO3 の非推奨の化学用語です。 .
別名:硝酸銀、月の結晶、銀の結晶
月の結晶 – 月の結晶は、固体の硝酸銀 (AgNO3 ).
ルテチウム – ルテチウムは、原子番号 71 のランタニド元素の名前で、記号 Lu で表されます。
リアーゼ – リアーゼは、分子に基を付加または除去して、加水分解または酸化以外のプロセスによって二重結合または新しい環を形成する反応を触媒する酵素です.
灰汁 – 灰汁は、化合物の水酸化ナトリウム (NaOH) の一般名です。
別名:水酸化ナトリウム、苛性ソーダ
ライマン シリーズ – ライマン級数は、主エネルギー準位 n> 1 から基底エネルギー準位 n =1 までの電子遷移に対応する、水素からの一連の紫外線輝線です。
リス – Lys は、アミノ酸のリジンの略語です。
リジンはKとも略されます。
A B C D E F G H I J K L M N O P Q R S T U V W X Y Z