その理由は次のとおりです。
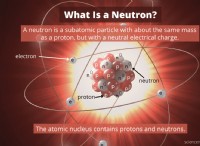
* 電子は反応性を決定します: 電子は負に帯電し、正に帯電した核の周りの軌道に存在します。これらの電子の配置、特に最も外側のシェル(価電子)の配置は、原子が他の原子とどのように相互作用するかを決定します。
* アトラクションと共有: 化学結合は、1つの原子の正に帯電した核と別の原子の負に帯電した電子の間の静電引力のために形成されます。原子は、電子を獲得、紛失、または共有することにより、より安定した構成を実現できます。
* 結合の種類:
* イオン結合: 1つの原子は電子を失い、積極的に帯電します(陽イオン)。反対に帯電したイオンは互いに引き付けます。
* 共有結合: 原子は電子を共有して安定した構成を実現し、分子を形成します。
* 金属結合: 電子は非局在化され、金属原子の格子間で共有されます。
要約すると、化学結合に重要な役割を果たすのは電子、特に価電子です。それらは、原子を一緒に保持して分子と化合物を形成する「接着剤」です。