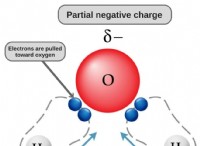
NaOHを水に加えると、水素イオン(H+)濃度 *減少 *が減少し、水酸化物イオン(OH-)濃度 *が増加します *。
その理由は次のとおりです。
* naohは強力なベースです。 これは、水中で完全に解離し、ナトリウムイオン(Na+)および水酸化物イオン(OH-)を放出することを意味します。
* oh-イオンの添加は、水の自己固定の平衡をシフトします。 水分子は陽子を寄付して受け入れることができます(H+)。平衡反応は次のとおりです。
`` `
2 H2O <=> H3O + + OH-
`` `
* le Chatelierの原則。 OHIONIONを追加すると平衡が左に押し出され、H3O+(ヒドロニウム)イオンの一部がOHIONIONと反応してより多くの水分子を形成します。これにより、H+イオンの濃度が低くなります。
要約: NaOHを水に追加すると、水酸化物イオン(OH-)の濃度が増加し、水素イオン(H+)の濃度が減少します。これは、NaOHが水酸化物イオンを放出する強力な塩基であり、加えられた水酸化物イオンが濃度を減らすためにヒドロニウムイオンと反応するためです。