* 電子構成: 炭素の原子番号は6個です。つまり、6個のプロトンと6個の電子を備えています。その電子構成は1S²2S²2p²です。
* 価電子: 価電子は、原子の最も外側の殻の電子であり、化学結合に関与しています。炭素の最も外側のシェル(2番目のシェル)には4つの電子があります(2S軌道に2つ、2p軌道に2つ)。
* 結合する傾向: 炭素は、最も外側のシェルで安定したオクテット(8電子)を達成するために、電子を獲得、失い、または共有する傾向があります。これを達成するには、4つの電子を獲得または共有する必要があります。
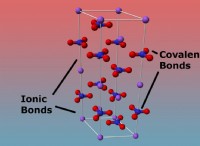
* Tetravalency: 炭素はオクテットを完成させるためにさらに4つの電子を必要とするため、 4つの共有結合を形成します 、それをテトラバレントにします。
簡単に言えば、炭素は外側のシェルに4つの「空のスロット」を持っているため、他の原子と電子を共有することで満たすことができます。 4つの結合を形成するこの能力は、炭素を非常に用途が広く、生命に不可欠なものにしています。