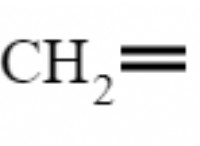水(h₂o)
* ハイブリダイゼーション: 水中の酸素原子はSp³ハイブリダイゼーションを受けます。つまり、その4つの原子価電子が4つのハイブリッド軌道を占めています。これらの軌道のうち2つは2つの水素原子とSigma結合を形成し、他の2つの軌道には電子の孤立ペアが含まれています。
* 孤立ペア: 酸素原子の電子の孤独なペアは結合ペアを撃退し、水素原子を近くに押し込み、曲がったまたはV字型のジオメトリを作成します。
* 結合角: 水中のH-O-H結合角は約104.5°で、孤立ペアからの反発により、109.5°の理想的な四面体角よりわずかに少ないです。
二酸化炭素(Co₂)
* ハイブリダイゼーション: 二酸化炭素の炭素原子はSPハイブリダイゼーションを受け、2つのSPハイブリッド軌道をもたらします。各SPハイブリッド軌道は、酸素原子とSigma結合を形成します。
* 線形ジオメトリ: 2つのシグマ結合は線形に配置され、中央に炭素原子と両側に2つの酸素原子があります。
* 結合角: 二酸化炭素のO-C-O結合角は180°です。
要約:
* 水: 結合ペアを撃退し、V字型のジオメトリを作成する酸素原子に2つの孤立ペアが存在するため、曲がった形状。
* 二酸化炭素: 炭素原子のSPハイブリダイゼーションと中心炭素原子の孤立ペアの欠如による線形形状により、原子の線形配置が生じます。
この形状の違いは、これらの分子の特性に直接影響します。 Waterの曲がった形状は、強い双極子モーメントを備えた極地分子になり、水素結合を可能にし、高い表面張力や優れた溶媒機能などのユニークな特性を提供します。一方、二酸化炭素は線形および非極性分子であるため、溶媒が不十分で、温室効果ガスとしての役割に貢献しています。